
Reportáže a rozhovory z odborných kongresů
Těžká chronická rinosinusitida s nosními polypy (CRNP) představuje mnohdy frustrující diagnózu – navzdory intranazálním a systémovým kortikoidům i opakovaným operacím zůstává řada pacientů výrazně symptomatická a funkčně limitovaná. Studie WAYPOINT (Lipworth BJ et al., N Engl J Med 2025) poprvé ukazuje, že blokáda epitelového alarminu TSLP pomocí biologika tezepelumabu dokáže významně zmenšit objem polypů, zmírnit nosní kongesci, zlepšit čich i celkovou kvalitu života a zároveň snížit potřebu podávání systémových kortikoidů a indikování chirurgických zákroků. Jako „upstream“ biologikum zasahující do časné fáze zánětlivé kaskády navíc překračuje tradiční úzké vymezení čistě eozinofilního typu 2 a otevírá cestu k personalizovanější, fenotypově méně omezené léčbě CRNP.
Chronická rinosinusitida s nosními polypy (CRNP) je heterogenní zánětlivé onemocnění horních dýchacích cest. Patogeneze tohoto stavu je charakterizována dysfunkcí epiteliální bariéry a zánětlivými mechanismy typu 2, do nichž jsou zapojeny upstream epiteliální cytokiny, jako je tymický stromální lymfopoetin (TSLP) a interleukin 33 (IL-33). Upstream epiteliální cytokiny jsou skupinou signalizačních proteinů rychle uvolňovaných epitelovými buňkami (například v plicích, kůži, střevech) jako první reakce na poškození tkáně, kontakt s alergeny, patogeny nebo dráždivými látkami ze zevního prostředí. Označení „upstream“ zdůrazňuje jejich pozici na začátku zánětlivé kaskády – působí jako alarminy neboli signály nebezpečí, které okamžitě mobilizují a směrují následnou imunitní odpověď.
U pacientů je toto onemocnění spojeno s nepříjemnými symptomy zahrnujícími nosní kongesci, bolest v obličeji, ztrátu čichu, poruchy spánku a únavu, které vážně ovlivňují kvalitu života. Standardní léčba, včetně intranazálních kortikoidů, mívá na velikost nosních polypů a symptomy leckdy jen omezený účinek. U pacientů s těžkou, recidivující CRNP bývají proto často indikovány opakované sinonazální chirurgické zákroky nebo záchranná (rescue) terapie systémovými kortikoidy. Přestože se biologická léčba, zaměřená na zánětlivé dráhy typu 2 (například IL-5, IL-4, IL-13 a IgE), ukázala jako nová terapeutická možnost, stále existuje neuspokojená potřeba týkající se těch nemocných, kteří na stávající biologické účinné látky adekvátně nereagují.
TSLP (tymický stromální lymfopoetin) je jedním z klíčových faktorů řídících zánětlivé kaskády. Jeho zvýšené hladiny byly zjištěny ve tkáňových vzorcích nosních polypů u pacientů s CRNP. Tezepelumab je humánní monoklonální protilátka, která specificky blokuje interakci TSLP s jeho heterodimerním receptorem. Tato látka se již dříve osvědčila u pacientů s těžkým, nekontrolovaným astmatem. Fáze III studie NAVIGATOR již naznačila, že léčba tezepelumabem vede ke klinicky významnému snížení sinonazálních symptomů u pacientů s astmatem a komorbidní CRNP.
Cílem mezinárodní multicentrické, paralelně skupinové, dvojitě zaslepené, randomizované, placebem kontrolované studie fáze III WAYPOINT (Lipworth BJ et al., N Engl J Med 2025) bylo posoudit účinnost a bezpečnost tezepelumabu u dospělých pacientů s těžkou, nekontrolovanou CRNP.
Celkem bylo randomizováno 410 jedinců, přičemž do analýz účinnosti a bezpečnosti bylo zařazeno 408 nemocných (203 ve skupině s tezepelumabem a 205 s placebem). Všichni dostávali standardní péči, včetně intranazálních kortikoidů. Tezepelumab (v dávce 210 mg) nebo placebo byly podávány subkutánně každé 4 týdny po dobu 52 týdnů. Primární cílové ukazatele studie hodnotily změnu od výchozího stavu po 52 týdnech v:
Klíčové sekundární cílové ukazatele zahrnovaly: skóre ztráty čichu, celkové skóre Sinonasal Outcome Test (SNOT-22; rozsah 0–110), skóre Lund-Mackay (hodnotí opacity dutin na CT, rozsah 0–24) a čas do prvního rozhodnutí o léčbě (chirurgie nebo systémové kortikoidy).
Většina zařazených pacientů trpěla závažným onemocněním, průměrná doba od diagnózy byla téměř 12,8 roku. U 71,3 % sledovaných už byla provedena předchozí operace nosních polypů a 60,8 % trpělo komorbidním astmatem.
Ve studii WAYPOINT bylo prokázáno, že léčba tezepelumabem vedla k významnějším redukcím velikosti nosních polypů, závažnosti nosní kongesce a sinonazálních symptomů ve srovnání s placebem.
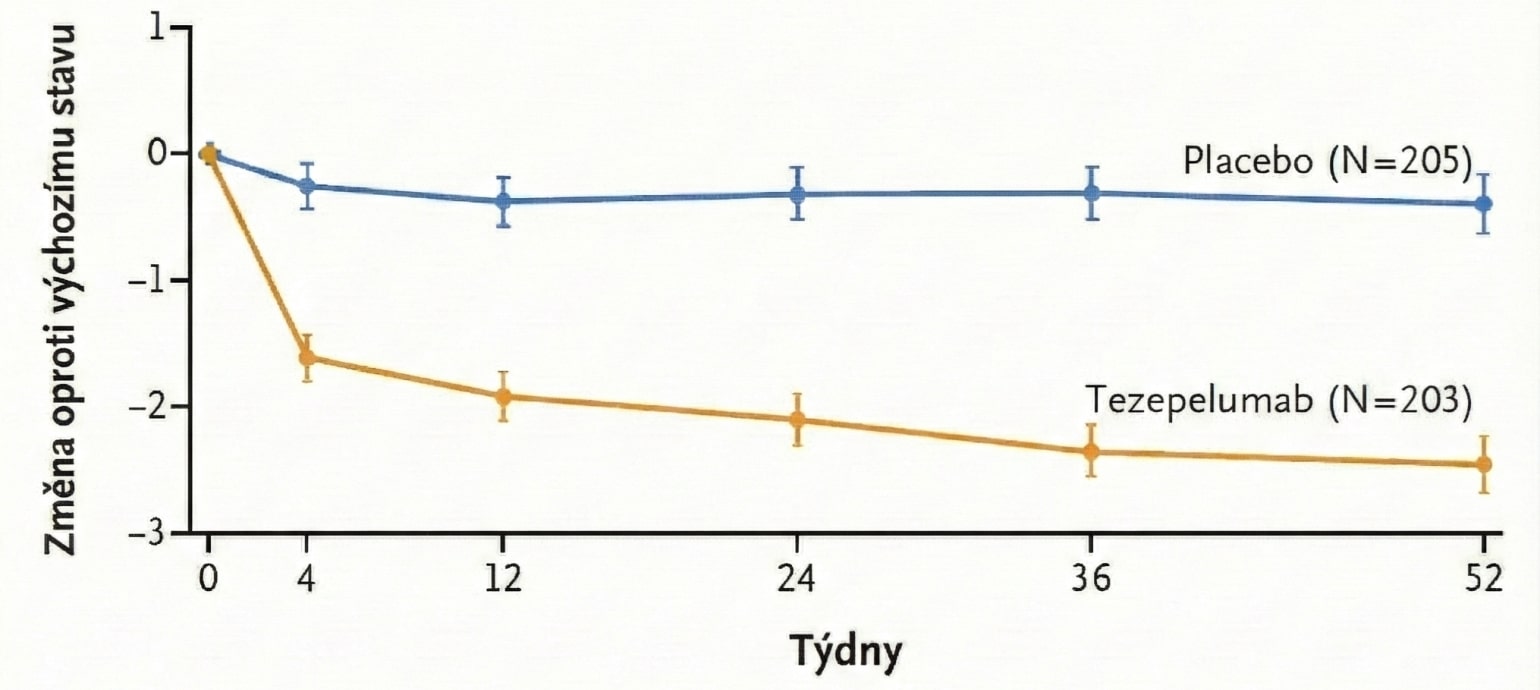
Pacienti užívající tezepelumab vykazovali významné zlepšení oproti placebu (průměrný rozdíl −2,07; p < 0,001). Zlepšení bylo pozorováno již od prvního posouzení po podání terapie (4. týden) a bylo udržováno po celých 52 týdnů.
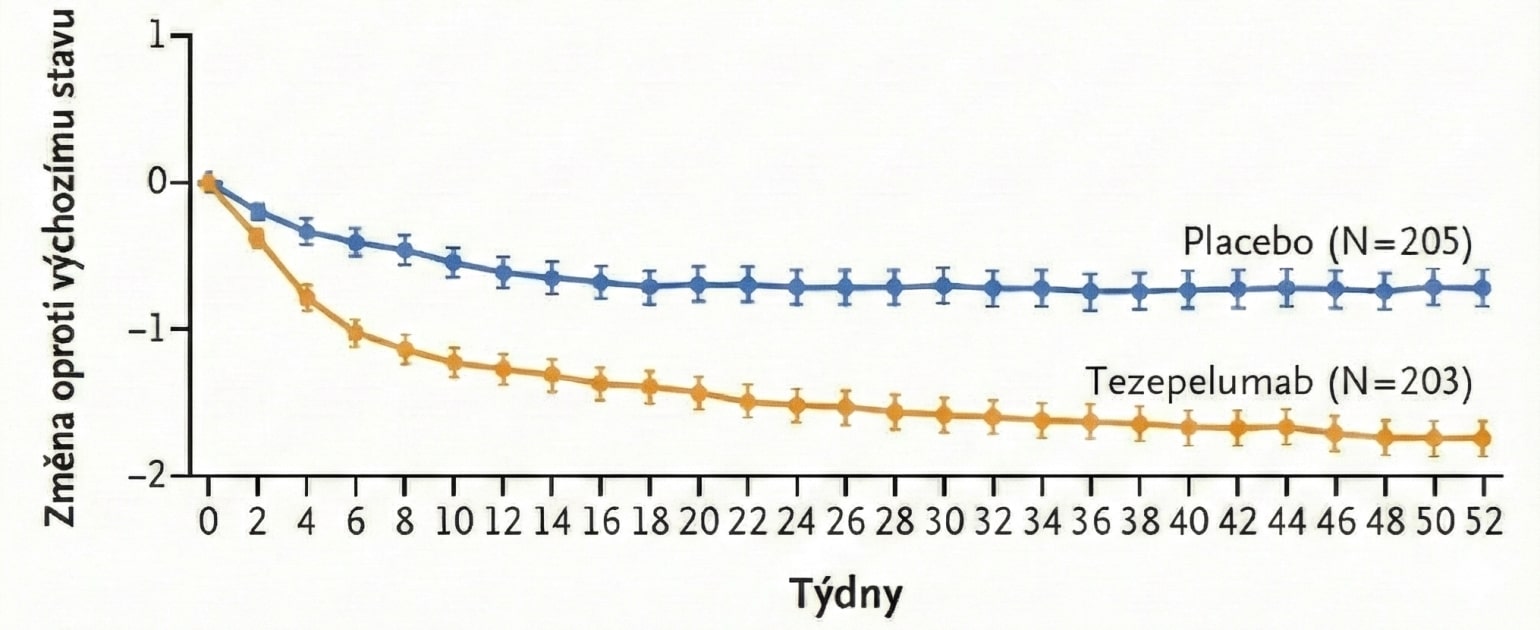
Zlepšení bylo rovněž významné (průměrný rozdíl oproti placebu −1,03; p < 0,001). Zlepšení kongesce bylo zaznamenáno dříve, již od 2. týdne.
Tezepelumab vedl k signifikantnímu zlepšení napříč všemi klíčovými hodnoceními symptomů.
Signifikantní zlepšení (průměrný rozdíl oproti placebu −1,00; p < 0,001). Lepší výsledky byly potvrzeny i v rámci testu identifikace čichu UPSIT (průměrný rozdíl 9,46).
Došlo k výraznému zlepšení kvality života a snížení příznaků (průměrný rozdíl oproti placebu −27,26; p < 0,001).
Snížení opacity dutin na CT skenech (průměrný rozdíl oproti placebu −5,72; p < 0,001).
Léčba tezepelumabem zásadně zredukovala potřebu záchranné léčby a chirurgických zákroků.
Během 52 týdnů byla operace indikována u výrazně menšího počtu pacientů ve skupině s tezepelumabem (pouze 0,5 %) ve srovnání se skupinou s placebem (22,1 %).
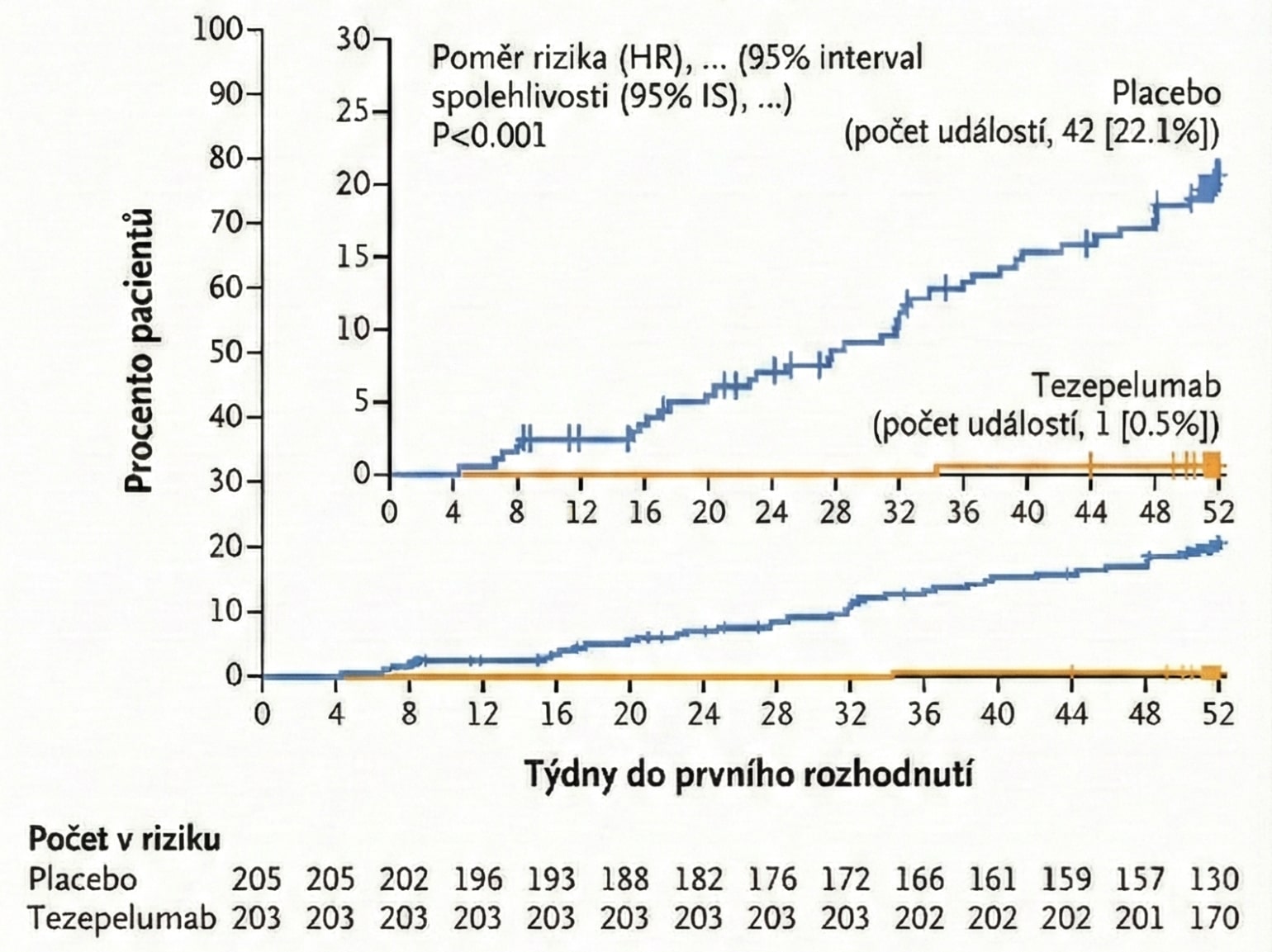
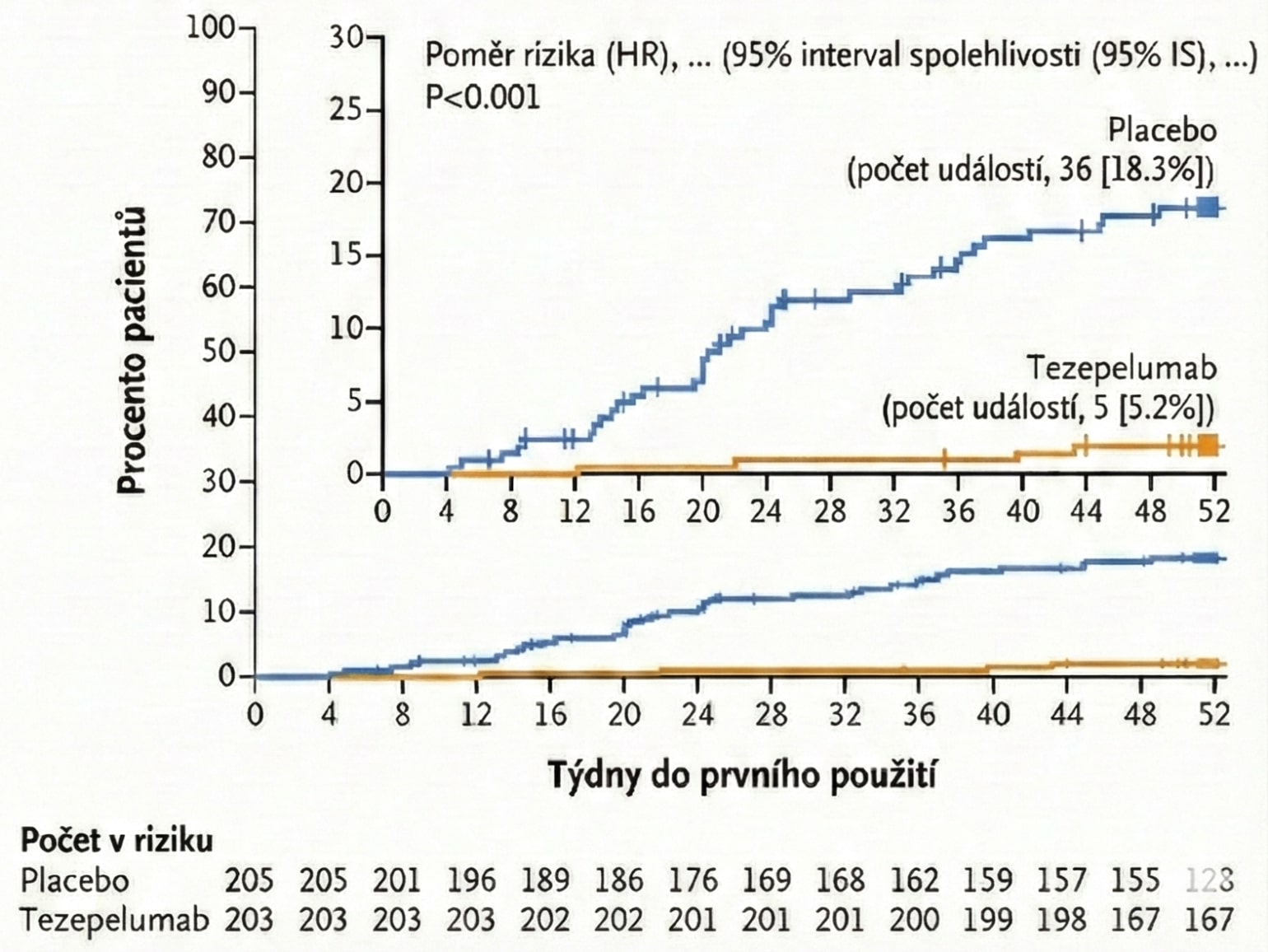
Užívání systémových kortikoidů bylo významně nižší ve skupině s tezepelumabem (5,2 %) než ve skupině s placebem (18,3 %), což dokládá i poměr rizik (hazard ratio) 0,12 (95% CI; 0,04–0,27). Rozdíl mezi oběma skupinami je významnější u tezepelumabu po celou dobu trvání studie (p < 0,001). Tato redukce je klinicky velmi významná kvůli závažným nežádoucím účinkům kortikoidů.
Celkový výskyt nežádoucích účinků byl srovnatelný mezi oběma skupinami (78,3 % ve skupině s tezepelumabem vs. 77,1 % ve skupině s placebem).
Studie fáze III WAYPOINT prokázala, že léčba tezepelumabem vede, ve srovnání s placebem, k výraznějším redukcím velikosti nosních polypů a závažnosti nosní kongesce u dospělých s těžkou, nekontrolovanou CRNP. Tento terapeutický přístup, zaměřený na blokádu upstream cytokinu TSLP, vedl k signifikantnímu snížení symptomů hlášených pacienty (včetně zlepšení čichu a celkové kvality života dle SNOT-22) a zásadně redukoval potřebu chirurgického zákroku a použití systémových kortikoidů.
Výsledky naznačují, že biologická léčba, která se zaměřuje na TSLP, by mohla vést k modifikaci onemocnění a k potenciální remisi u pacientů s těžkou CRNP, podobně jako u jiných zánětlivých onemocnění, jako je těžké astma. Biologické terapie představují zásadní posun od pouhého potlačování symptomů k ovlivňování základních zánětlivých mechanismů.
(red)
Zdroj

Reportáže a rozhovory z odborných kongresů
Opouštíte prostředí společnosti Pfizer, spol. s r. o.
Společnost Pfizer, spol. s r. o., neručí za obsah stránek, které hodláte navštívit.
Přejete si pokračovat?