
Reportáže a rozhovory z odborných kongresů
Zatímco v Evropě přístup k novinkám v léčbě atopické dermatitidy (AD) spíše stagnuje, v USA je situace jiná. Ruxolitinib, roflumilast a tapinarof – to jsou tři nejnovější topicky používaná léčiva, která za sebou mají úspěchy ve velkých studiích fáze III. Také do systémové léčby AD zavanul čerstvý vítr. Nakolik jsou nemolizumab, rocatinlimab, telazorlimab a amlitelimab efektivní? Na to přinášejí odpověď následující řádky.
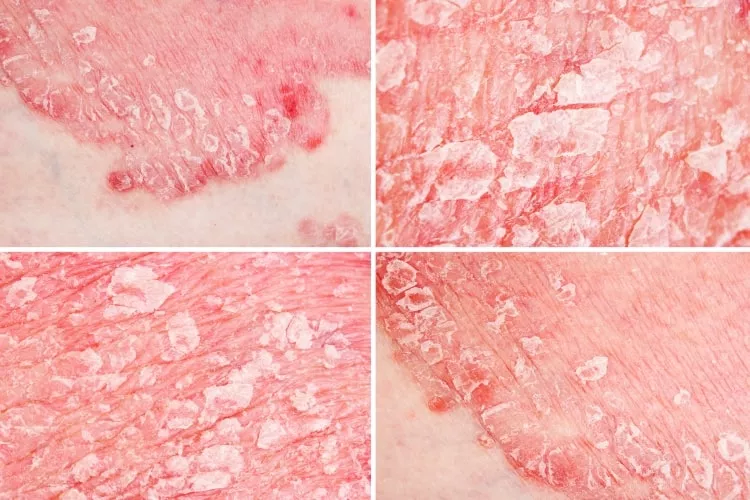
Před začátkem úvah o efektivitě jednotlivých léčiv je třeba si uvědomit, že studie provedené s ruxolitinibem, roflumilastem a tapinarofem nelze vzájemně srovnávat, protože byly zaměřeny na velmi rozdílné populace za výrazně odlišných podmínek. Zatímco ruxolitinib byl podáván pacientům starším 12 let, přičemž 80 % zkoumané populace tvořili dospělí, u tapinarofu byla většina zkoumaných jedinců dětského věku (nejmladší pacienti měli jen 2 roky). Pomocí roflumilastu byli léčeni jedinci starší 6 let, průměrný věk ve studii činil 28 let. V jednotlivých studiích se lišil rozsah plochy postižení (BSA – body surface area) i jeho závažnost (dle skóre IGA – Investigator Global Assessment). Zatímco pacienti léčení ruxolitinibem měli BSA mezi 3–20 %, někteří nemocní léčení roflumilastem dosahovali i BSA 100 %. Tapinarof byl zase jediným léčivem, které bylo použito též u pacientů s nejtěžším IGA.
Do studie zaměřené na účinnost inhibitoru JAK proteinové kinázy ruxolitinibu byli zařazeni pacienti s maximálním BSA 20 % a mírnou nebo střední závažností AD dle skóre IGA, jimž bylo 12 let a více. Následně došlo k randomizaci v poměru 2 : 2 : 1. V první skupině byli nemocní léčení ruxolitinibem v koncentraci 0,75 % aplikovaném dvakrát denně (BID). Druhá skupina dostávala ruxolitinib v koncentraci 1,5 % BID. Ve třetí, kontrolní skupině bylo místo aktivního léku použito k lokální léčbě AD pouze vehikulum.
Prvních 8 týdnů studie probíhalo následovně: Pacienti randomizovaní na ruxolitinib setrvali u této léčby, jedinci z kontrolní skupiny byli randomizováni 1 : 1 k užívání ruxolitinibu v koncentraci 0,75 % nebo 1,5 %. Kontroly probíhaly každé 4 týdny po následujících 44 týdnů.
Jak to dopadlo? Zatímco u pacientů z kontrolní skupiny dosáhlo IGA 0/1 asi 15 %, ve skupině léčené ruxolitinibem šlo o 50 % v případě ruxolitinibu v koncentraci 0,75 % a o 53 % v koncentraci 1,5 %. Efektivita léku je tedy zřejmá. Obdobné výsledky byly pozorovány i v jiných pracích s ruxolitinibem a v odlišných věkových skupinách. Léčivo také vedlo ke signifikantnímu snížení pruritu – a to již po několika dnech používání. U mnoha nemocných bylo významné zlepšení svědění pozorováno už po jednom dni! Průměrný pokles pruritu hodnoceného pomocí skóre NRS (Numerical Rating Scale) činil až –3,39 v případě užití 1,5% ruxolitinibu a –2,81 u skupiny užívající 0,75% ruxolitinib. V jedné menší studii, kde byl ruxolitinib použit u 48 pacientů v režimu open-label, byla již po 15 minutách od aplikace změřena signifikantně nižší míra pruritu a také hodnoty některých biomarkerů.
Nejčastějšími nežádoucími účinky (NÚ), které se při léčbě ruxolitinibem vyskytly, byly nazofaryngitidy a infekce horních dýchacích cest. Nejvýznamnější limitací je u použití ruxolitinibu plocha postižení – lze jej užít jen u pacientů s BSA 20 % a méně (Papp K et al., J Am Acad Dermatol. 2021;85:863–872).
Dalším novým léčivem použitelným v lokální léčbě AD je inhibitor PDE4 roflumilast. Zatímco v tabletách je tento lék určen k udržovací léčbě chronické obstrukční plicní nemoci (CHOPN) s častými exacerbacemi, ve verzi krému je v USA a Kanadě schválen v koncentraci 0,3 % k léčbě psoriázy a v koncentraci 0,15 % k léčbě AD (u pacientů starších šesti let).
Výsledky multicentrické, dvojitě zaslepené, randomizované, vehikulem kontrolované studie fáze III, která zkoumala efektivitu roflumilastu v léčbě AD mírné nebo střední intenzity, byly zveřejněny v roce 2023. Bylo do ní zařazeno 1 337 pacientů starších šesti let, kteří byli následně randomizováni v poměru 2 : 1 na léčbu roflumilastem v koncentraci 0,15 % a aplikaci prostého vehikula. Jejich BSA činilo více než 3 % a skóre EASI bylo vyšší než 5. Po čtyřech týdnech užívání dosáhlo 32 % pacientů významného snížení skóre vIGA-AD (Validated Investigator Global Assessment for AD), v kontrolní skupině šlo pouze o 15 %.
Maximální efektivita léku byla ještě vyšší, ale bylo jí dosaženo až po delší době užívání. Roflumilast vykázal podobně dobré výsledky též u dětí mezi 2–5 roky, kde snížení vIGA-AD po 4 týdnech činilo 25,4 %. Co se týče zlepšení pruritu, rozdíl mezi vehikulem a aktivním léčivem byl viditelný již po jednom dni, maximálního efektu bylo dosaženo v průběhu 2 týdnů. Nejčastějšími nežádoucími účinky byly bolesti hlavy, nauzea, průjem a zvracení, projevily se však u velmi nízkého počtu pacientů (1,2–3,5 %). Popisované příznaky odpovídaly výskytu nejčastějších nežádoucích účinků roflumilastu při systémové léčbě.
Agonista AhR (aryl hydrocarbon receptor) tapinarof je v podobě krému schválen v USA k léčbě psoriázy. V případě AD je jeho mechanismus fungování zřejmý – pomocí navýšení množství koncentrace komponent kožní bariéry (zejména ceramidů) vede ke zlepšení její funkce. Současně snižuje koncentraci zánětlivých cytokinů a oxidativní stres (Bissonnette R et al., J Am Acad Dermatol. 2021;84:1059–1067).
Studie fáze III zkoumající efektivitu tapinarofu byly dvě, prakticky identické. Do obou byli zařazeni pacienti starší dvou let, se skórem vIGA-AD nad 3, skórem EASI nad 6 a BSA 5–35 %, v počtu 407 a 406. V obou studiích byli nemocní randomizováni 2 : 1 k 8 týdnů trvající, dvojitě zaslepené léčbě buď tapinarofem v koncentraci 1 % nebo samotným vehikulem (Silverberg JI et al., J Am Acad Dermatol. 2024;91:457–465). Pacientů, jimž se podařilo dosáhnout IGA 0/1, bylo na tapinarofu 45,4 %, respektive 46,4 % ve druhé studii. Na vehikulu byla taková odpověď popisována u 13,9 % a 18,0 %. Z hlediska nežádoucích účinků byly nejčastější folikulitidy, někdy s hnisem, někdy spíše podobné keratosis pilaris, a bolesti hlavy (Bissonnette R et al., J Eur Acad Dermatol Venereol. 2023;37:1168–1174).
U léčby tapinarofem je velmi zajímavé, jak dlouho trvá její efekt i po skončení podávání. Ve studii, do níž byli zařazeni jedinci s psoriázou léčenou tapinarofem, byl medián délky efektu po ukončení používání krému 115 dní.
Pro pacienty se závažnými projevy AD existují i nové možnosti systémové léčby. Protilátkou, kterou by mohlo být možno využít k systémové léčbě AD, je nemolizumab. Jde o protilátku proti IL-31, která je v USA schválena pro léčbu prurigo nodularis a již má za sebou studie fáze III pro indikaci AD. Ve studii byla efektivita nemolizumabu srovnávána s topickými kortikoidy (TCS), oproti nimž nemolizumab prokázal signifikantní zlepšení. Pokles pruritu byl znatelný už po jednom týdnu od prvního podání nemolizumabu. U některých nemocných se při užívání nemolizumabu objevily edémy.
Naprostou novinkou, která je momentálně zkoumána ve studiích a ještě neprošla schválením, jsou různé protilátky proti OX40 (rocatinlimab, telazorlimab), molekuly nacházející se na T-buňkách a proti ligandu OX40 (amlitelimab), který lze nalézt u buněk prezentujících antigen.
Telazorlimab je momentálně zkoumán ve studiích fáze III a podle dosavadních zjištění vede u některých pacientů k silnému a dlouhodobému efektu, který trvá i dva roky od posledního podání léčiva. Ve studii fáze II, do níž bylo v každém rameni zařazeno 78 dospělých pacientů se středně závažnou až závažnou AD, vedla dávka úvodní 1 200 mg telazorlimabu (a pokračovací dávka 600 mg jednou za dva týdny) po 16 týdnech k zásadnímu zlepšení příznaků. V 16. týdnu sledování nicméně ještě nebylo dosaženo vrcholného efektu; ten nastal až kolem 54. týdne, kdy byl u nemocných pozorován pokles EASI o téměř 90 %. Žádné zásadní nežádoucí účinky nebyly popisovány (Rewerska B et al., J Allergy Clin Immunol Glob. 2024;3:100195).
Rocatinlimab je anti-OX40 monoklonální protilátka, která dokáže indukovat na protilátce nezávislou buněčnou toxicitu na T-buňkách. Momentálně je zkoumána ve studiích fáze III pro použití v léčbě AD. Ve studiích fáze II již prokázala velmi dobrý efekt trvající i týdny po vysazení léčiva, a to ve všech testovaných dávkováních (150 mg, 600 mg jednou za 4 týdny, 300 mg nebo 600 mg jednou za 2 týdny). Z nežádoucích účinků se objevila u více než 10 % nemocných horečka, zimnice, v případě nejvyššího dávkování šlo až o 20 %. Pacienti popisovali také aftózní vředy (Guttman-Yassky E et al., Lancet. 2023;401:204–214).
Ohledně rocatinlimabu už vyšly i první výsledky studie fáze III. Po 24 týdnech sledování dosáhlo EASI-75 32,8 % nemocných oproti 13,7 % s placebem, vIGA-AD 19,3 % oproti 6,6 % v kontrolní skupině a rIGA 0/1 16,4 % oproti 4,9 % v rameni s placebem. Jde tedy o statisticky signifikantní rozdíly. Je pravděpodobné, že nejde o konečná data – po 24 týdnech ještě nejspíš nebylo dosaženo plného efektu léčiva.
Poslední z nově zkoumaných systémových možností terapie je anti-OX40L protilátka amlitelimab. Ve studii fáze II byli pacienti s amlitelimabem randomizováni do čtyř skupin s různým dávkováním, pátá skupina byla kontrolní. Celkem šlo o 589 nemocných. Primárním endpointem byla procentuální změna EASI od počátku studie do 16. týdne. Následně byli nemocní randomizováni k ukončení léčby amlitelimabem a přechodu na placebo nebo k pokračování terapie. Amlitelimab jednoznačně prokázal svou efektivitu oproti placebu, rozdíly začaly být zřejmé mezi 4. a 8. týdnem užívání. Po 24 týdnech od konce užívání léčiva byl u více než poloviny pacientů, u nichž došlo vlivem léčby amlitelimabem k dosažení IGA 0/1, zachován efekt. Stran nežádoucích účinků nebyly pozorovány významné rozdíly mezi aktivním léčivem a placebem.
Možnosti léčby AD se budou rozšiřovat a již teď je zřejmé, že mnoha směry. Novinky existují jak v oblasti lokální léčby, tak systémové terapie. Zbývá jen otázka, kdy a jak se tyto nové léky dostanou do běžné klinické praxe.
Redakčně zpracováno ze sdělení, které na výročním kongresu EADV, konaném 25.–28. září 2024 v Amsterdamu, přednesl:
Robert Bissonnette, MD, FRCPC
Innovaderm Research, Montreal, Kanada




Reportáže a rozhovory z odborných kongresů
Opouštíte prostředí společnosti Pfizer, spol. s r. o.
Společnost Pfizer, spol. s r. o., neručí za obsah stránek, které hodláte navštívit.
Přejete si pokračovat?