
Reportáže a rozhovory z odborných kongresů
prof. MUDr. Martin Prázný, CSc., Ph.D.
III. interní klinika – klinika endokrinologie a metabolismu 1. LF UK a VFN v Praze
Glifloziny a inkretinová mimetika nejen kontrolují glykemii, ale nabízejí také přídavné kardiální a renální benefity. Mohou zpomalit progresi chronického onemocnění ledvin a snížit riziko kardiovaskulárních příhod. Co přináší jejich vzájemná kombinace pro pacienty s diabetem 2. typu a vysokým kardiometabolickým rizikem?
V terapii snižující hyperglykemii u diabetu 2. typu (DM2) lze tradičně využít jak mechanismy závislé na inzulinu, tak nezávislé na jeho působení. Mezi první skupinu léků patří inzulinové senzitizéry (metformin nebo thiazolidindiony), inzulinová sekretagoga (deriváty sulfonylurey, GLP-1 agonisté, inhibitory DPP-4 a glinidy) a také inzulinoterapie zajišťující náhradu fyziologického inzulinu. Ačkoliv jsou tato tradiční antidiabetika účinná, jejich podávání může být spojeno s rizikem hypoglykemií a nárůstu hmotnosti nebo závisí na dostatečné rezervě beta-buněk pankreatu.
Léky nezávislé na inzulinu, zejména inhibitory SGLT2 (SGLT2i) neboli glifloziny, pak nabízejí skvělou možnost pro kombinační terapii, která využívá různých mechanismů účinku. Důležitou vlastností gliflozinů je jejich nezávislost na inzulinové signalizaci, což umožňuje jejich účinnost též u pacientů s pokročilým diabetem, u nichž často dochází ke ztrátě funkce beta-buněk pankreatu.
Mluví-li se dnes o moderní kombinační antidiabetické léčbě, jde hlavně o kombinaci SGLT2i a agonistů receptoru pro GLP-1 (GLP1-RA), protože tyto léky mají jak významný antidiabetický efekt, tak přídavné neglykemické účinky, kterými lze ovlivnit průběh samotného diabetu i rozvoj pozdních komplikací. Pojďme se na výhody obou těchto léků podívat podrobněji.
Připomeňme, že glifloziny inhibují sodíko-glukózový kotransportér 2 v proximálním tubulu ledvin, který je zodpovědný za renální reabsorpci glukózy. Inhibice tohoto mechanismu vede ke glykosurii a tím také ke kalorické ztrátě, což u diabetika zprostředkuje snížení glykemie a zlepšení jeho kompenzace (antidiabetický efekt). Kromě toho bylo prokázáno, že podávání gliflozinů vede také ke snížení krevního tlaku, hmotnosti a poklesu albuminurie a zlepšuje tak prognózu pacientů s kardiovaskulárními (KV) i renálními onemocněními.
Odborníci zpočátku k SGLT2i přistupovali s nedůvěrou, protože existovaly obavy, jak bude tento mechanismus v ledvinách vlastně fungovat a co bude nadměrná glykosurie způsobovat v močových cestách. Ukázalo se, že tyto pochybnosti nebyly opodstatněné. Přirozená inhibice SGLT2 nemá u lidí, kteří mají vyřazeny geny pro SGLT2, žádné negativní dopady. Naopak, zjistilo se, že jim inhibice SGLT2 prospívá.
Klinické studie, například s dapagliflozinem, ale prokázaly i další pozitivní neglykemické účinky v podobě kardioprotekce a renoprotekce u pacientů se srdečním selháním (HF) a chronickým onemocněním ledvin (CKD), a to i u nemocných bez diabetu. Například European Renal Association dnes doporučuje SGLT2i jako standardní léčbu u pacientů s CKD, protože zlepšují renální parametry, zpomalují zhoršení glomerulární filtrace, snižují albuminurii a zpomalují progresi selhání ledvin do dialýzy.
Jak výrazný je renoprotektivní efekt gliflozinů, ilustrují například výsledky post hoc analýzy studie DAPA-CKD (Schechter M et al. Ann Intern Med. 2023;176:59–66), která hodnotila vliv léčby dapagliflozinem na hospitalizace u pacientů s CKD bez ohledu na přítomnost diabetu. Dapagliflozin ve srovnání s placebem snížil riziko první hospitalizace o 16 % (HR = 0,84; 95% CI, 0,75–0,94) a redukoval celkový počet hospitalizací nebo úmrtí o 21 % (RR = 0,79; 95% CI, 0,70–0,89). Pro zabránění jedné hospitalizace je přitom nutné léčit dapagliflozinem pouze 23 nemocných (NNT = 23). Riziko hospitalizací z jakékoliv příčiny bylo ve skupině s dapagliflozinem nižší o 22 % ve srovnání s placebem (RR = 0,78; 95% CI, 0,70–0,87). Tyto účinky byly konzistentní bez ohledu na přítomnost DM2.
Pro větší ilustraci dlouhodobého efektu dapagliflozinu byla provedena analýza, která extrapolovala výsledky studie DAPA-CKD na období 10 let. Vyplývá z ní, že přidání dapagliflozinu ke standardní péči pacientů s CKD by mohlo vést k významnému zpomalení progrese CKD, čímž by se při léčbě 1 000 pacientů v horizontu 10 let zabránilo 83 úmrtím z jakékoli příčiny a 19 hospitalizacím pro srdeční selhání. Podání dapagliflozinu 1 000 pacientům po dobu 10 let by také vedlo k oddálení zahájení dialýzy či nutnosti transplantace u 51 nemocných a k redukci náhlého poklese renální funkce u 39 pacientů. Celkem to znamená, že z tisícovky pacientů by 109 žilo lepší život bez výskytu uvedených KV a renálních příhod. Tyto predikované dlouhodobé přínosy dapagliflozinu tak mají významné implikace pro klinickou praxi.
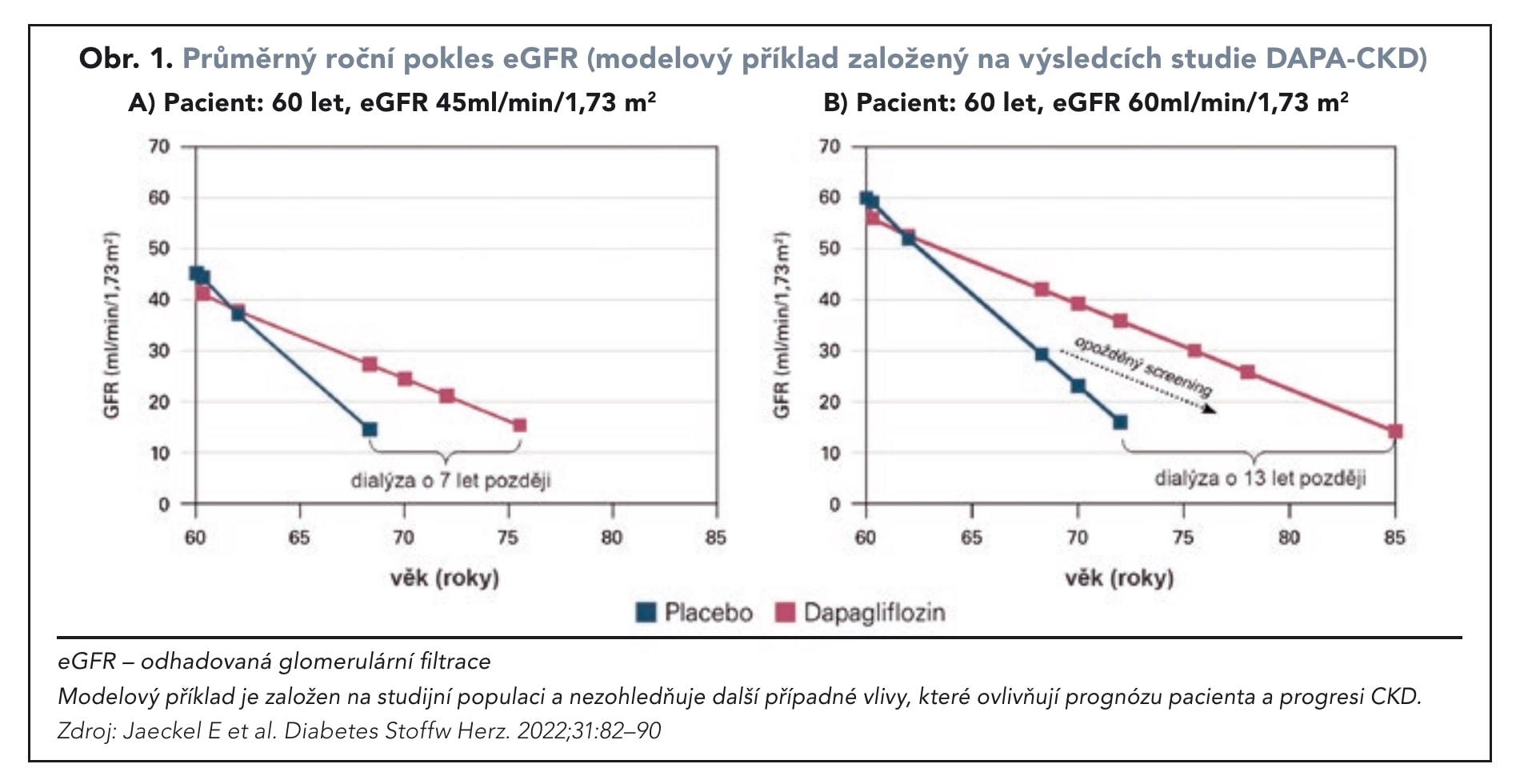
Data říkají, že dapagliflozin by se měl u CKD podat co nejdříve. Ve studii DAPA-CKD byl u dapagliflozinu pozorován průměrný roční pokles eGFR o 1,92 ml/min/1,73 m2 v porovnání s placebem. Znamená to, že pokud by byl takto dapagliflozinem léčen pacient ve věku 60 let s eGFR 45 ml/min/1,73 m2, pak by u něj došlo k hypotetickému oddálení nutnosti dialýzy o 7 let v porovnání s placebem. Jestliže by šlo o stejně starého nemocného, ale s eGFR 60 ml/min/1,73 m2, pak by se nutnost dialýzy oddálila hypoteticky dokonce o 13 let (obr. 1).
Diabetes 2. typu je komplexní systémové onemocnění, které zasahuje prakticky všechny orgánové systémy a významně ovlivňuje riziko pozdních komplikací. Proto se jeho léčba v posledních letech posouvá od výhradní kontroly glykemie ke strategiím, které současně ovlivňují i riziko pozdních komplikací. Kromě popsaného nefroprotektivního působení nabízí dapagliflozin také konzistentní přínos u pacientů se srdečním selháním napříč ejekční frakcí, jak dokládají výsledky studií DAPA-HF a DELIVER.
Vedle inhibitorů SGLT2 by podle recentních doporučení Americké diabetologické asociace (ADA) a Evropské asociace pro studium diabetu (EASD) měli být součástí iniciální terapie diabetiků 2. typu s aterosklerotickým kardiovaskulárním onemocněním také agonisté GLP-1, a to proto, že pozitivně ovlivňují nejen glykovaný hemoglobin a tělesnou hmotnost, ale mají také kardioprotektivní účinky, které jsou pravděpodobně zprostředkovány zejména zlepšením endoteliální funkce, snížením zánětlivých procesů a pozitivním vlivem na lipidový profil. Proto nepřekvapí, že u pacientů s diabetem 2. typu s vysokým kardiovaskulárním rizikem bylo při léčbě GLP-1 RA prokázáno snížení incidence velkých kardiovaskulárních příhod (MACE; zahrnuje infarkt myokardu, cévní mozkovou příhodu a KV úmrtí). Kromě KV benefitů vykazují GLP-1 RA také renoprotektivní účinky, které jsou pravděpodobně důsledkem snížení glomerulárního tlaku a zlepšení systémové hemodynamiky.
Agonisté GLP-1 mají významný vliv na glykemii i tělesnou hmotnost. Pokud jde o pokles glykovaného hemoglobinu, kromě inzulinu nemáme žádné jiné antidiabetikum s tak silným účinkem. Efekt závisí na dávce – vyšší dávky dosahují lepších výsledků, přičemž u některých pacientů lze pomocí GLP-1 RA dosáhnout snížení glykovaného hemoglobinu o více než 1,8 %.
Kromě toho moderní inkretinová mimetika, včetně GLP-1 RA, duálních agonistů GIP/GLP-1 a triple agonistů zahrnujících také ovlivnění glukagonových receptorů, prokázala vysokou účinnost při snižování tělesné hmotnosti u obézních pacientů s diabetem i bez něj (redukce tělesné hmotnosti o 15–20 %, což je významné nejen v léčbě samotného diabetu, ale také z hlediska populačního zdraví).
Přestože podání GLP-1 agonistů nebývá tradičně spojováno s nefroprotektivitou, tak i inkretinová mimetika (liraglutid, lixisenatid, semaglutid, dulaglutid) mají data potvrzující zpomalení nástupu albuminurie. Podobně pozitivní vliv na progresi albuminurie mají také SGLT2i, avšak například inhibitory DPP-4, kterými je v České republice ještě stále léčeno asi 110 000 diabetiků 2. typu, tímto renoprotektivním působením nedisponují. Renoprotektivní účinek inkretinových mimetik je naopak pozorován napříč GLP-1 agonisty ve srovnání s placebem.
Je otázkou, zda GLP-1 receptoroví agonisté mohou díky svým příznivým neglykemickým účinkům nahradit SGLT2i. Zdá se, že nikoliv. Mechanismy těchto dvou tříd léků nejsou plně zaměnitelné, jak naznačují například výsledky studie FLOW se semaglutidem u diabetiků s CKD. Z výsledků této studie mimo jiné vyplývá, že primární renální cíl byl semaglutidem ovlivněn ve všech skupinách pacientů kromě těch, kteří již byli předléčeni glifloziny. Podrobné vysvětlení tohoto výsledku si zaslouží ještě další analýzy, nicméně se zdá, že v léčbě diabetiků 2. typu se kombinace GLP-1 RA a SGLT2i jeví jako výhodnější strategie, která umožňuje lépe využít komplementárních mechanismů obou tříd léků.
V léčbě diabetiků 2. typu je kombinace GLP-1 RA a SGLT2i výhodnou strategií, která umožňuje lépe využít komplementárních mechanismů obou tříd léků.
V ideálním případě bychom měli začít léčbu co nejdříve, a to ještě před manifestací pozdních komplikací pacienta, abychom předešli zhoršení jeho stavu. Například dapagliflozin má pro to velmi silná data. Připomeňme, že studie DECLARE-TIMI 58 je nejrozsáhlejší KV studií v rámci SGLT2i s největším zastoupením pacientů v primární KV prevenci. Bylo do ní zařazeno 17 160 pacientů s diabetem 2. typu, kteří měli buď prokázané aterosklerotické KV onemocnění, nebo vícečetné rizikové faktory pro KV onemocnění, přičemž většinu (cca 60 %) představovali pacienti pouze s vysokým rizikem, ale bez manifestního KV onemocnění. Také z pohledu renálního postižení šlo o relativně „zdravější“ pacienty, neboť průměrná hodnota eGFR činila 85,2 ml/min/1,73 m2. Přesto pacienti léčení dapagliflozinem dosahovali konzistentně lepších výsledků z pohledu renálních specifických cílů bez ohledu na výchozí eGFR nebo UACR (poměr albuminu ke kreatininu v moči) v porovnání s placebem. Dapagliflozin v této nízkorizikové populaci také snížil relativní riziko kompozitu KV úmrtí nebo hospitalizace pro srdeční selhání o 17 %. Tento efekt byl převážně řízen redukcí hospitalizací pro srdeční selhání o 27 %. V podskupině diabetiků 2. typu se srdečním selháním s redukovanou ejekční frakcí studie také prokázala výrazné snížení jak kombinovaného parametru (hospitalizace pro srdeční selhání a KV úmrtí), tak samotné KV i celkové mortality. Studie DECLARE-TIMI 58 tím potvrdila účinnost léčby SGLT2i nejen v sekundární, ale i primární prevenci KV chorob. Metabolické zdraví mohou diabetologové zlepšit u všech diabetiků 2. typu i bez manifestního KV onemocnění (pouze s přítomnými rizikovými faktory, jako jsou hypertenze, obezita, dyslipidemie), kteří dostanou dapagliflozin. Možnost jeho kombinace s jakoukoli jinou léčbou diabetu, včetně inzulinu bazálního či v podobě intenzifikovaného inzulinového režimu, nahrává k většímu použití kombinace SGLT2i a GLP-1 RA, protože přináší jednoznačný potenciál zlepšit ještě více metabolické zdraví pacienta.
Studie DECLARE-TIMI 58 potvrdila přínos dapagliflozinu u pacientů v primární i sekundární prevenci kardiovaskulárních onemocnění.
Dapagliflozin je možné s úhradou předepsat širokému spektru pacientů s DM2 a sníženou renální funkcí (eGFR 25–75 ml/min/1,73 m2) bez ohledu na hladinu HbA1c a poměr albumin/kreatinin v moči (UACR).
(red)
Text byl zpracován podle sdělení, které zaznělo na sympoziu „A je to tu zas“ v hotelu Grandium v Praze 22. 11. – 23. 11. 2024.
Literatura

Reportáže a rozhovory z odborných kongresů
Opouštíte prostředí společnosti Pfizer, spol. s r. o.
Společnost Pfizer, spol. s r. o., neručí za obsah stránek, které hodláte navštívit.
Přejete si pokračovat?